Перейти к:
Лечение трижды негативного рака молочный железы у пациентки с метаболическим синдромом
https://doi.org/10.17709/2409-2231-2021-8-1-6
Аннотация
Рак молочной железы (РМЖ) остается одним из самых распространенных заболеваний женской части населения. По статистике РМЖ выявляется у каждой восьмой женщины. Приблизительно в 20–24% случаев от числа заболевших РМЖ диагностируется трижды негативный рак молочной железы. Для трижды негативного РМЖ характерно агрессивное клиническое течение, более высокая частота рецидивов и низкая общая выживаемость. По статистике медиана выживаемости женщин с метастатическим трижды негативным РМЖ составляет менее одного года. Мы демонстрируем успешный случай лечения женщины 60 лет, с диагнозом трижды негативный РМЖ справа, отечно‑инфильтративная форма, St IIIC cT4bN3M0 на фоне метаболического синдрома. Противоопухолевое лечение длилось 1 год, и состояло из трех этапов: системная химиотерапия, хирургическое лечение (радикальная мастэктомия), адъювантная лучевая терапия. После проведенного лечения достигнута ремиссия. Пациентка жива, безрецидивный период – 3 года.
Заключение. Не смотря на тяжелую сопутствующую патологию у наблюдаемой пациентки, мы получили положительный результат многоступенчатой терапии, где цитотоксическая химиотерапия была базовым лечением для женщины с трижды негативным РМЖ.
Ключевые слова
Для цитирования:
Ройтберг Г.Е., Дорош Ж.В., Аникеева О.Ю. Лечение трижды негативного рака молочный железы у пациентки с метаболическим синдромом. Research'n Practical Medicine Journal. 2021;8(1):62-68. https://doi.org/10.17709/2409-2231-2021-8-1-6
For citation:
Roitberg G.E., Dorosh J.V., Anikeeva O.Yu. Treatment of thrice-negative breast cancer in a patient with metabolic syndrome. Research and Practical Medicine Journal. 2021;8(1):62-68. (In Russ.) https://doi.org/10.17709/2409-2231-2021-8-1-6
ВВЕДЕНИЕ
Рак молочной железы (РМЖ) остается одним из самых распространенных заболеваний женской части населения [1][2][3][4]. По статистике РМЖ выявляется у каждой восьмой женщины [5]. В Российской Федерации на его долю приходится 20,9% от общего числа впервые выявленных случаев злокачественных опухолей [6]. Приблизительно в 20–24% случаев от числа заболевших РМЖ диагностируется трижды негативный рак молочной железы [7][8].
Актуальность исследований РМЖ и интерес к ним связаны не только с возросшим уровнем заболеваемости, но и с последующей высокой смертностью. Так, у женщин в возрасте до 40 лет РМЖ является основной причиной смертности [4][7]. Медиана выживаемости женщин с метастатическим трижды негативным РМЖ составляет менее одного года [9].
Гетерогенность опухолей репродуктивной системы и РМЖ, в частности, хорошо известна и обычно диагносцируется с использованием рутинных маркеров [10]. Клинически рак молочной железы обычно подразделяется на четыре подтипа в зависимости от наличия рецепторов к эстрогену, прогестерону, эпидермального фактора роста и индекса пролиферации (Ki‑67) [11][12]. Для трижды негативного РМЖ характерно отсутствие экспрессии к эстрогену, прогестерону, эпидермальному фактору роста [8][13].
В последнее время появились сообщения, что ожирение так же является фактором риска развития РМЖ [14][15]. Десятилетняя выживаемость при РМЖ у пациенток с ожирением значительно ниже по сравнению с женщинами с нормальным весом: относительный риск – 1,34 (доверительный интервал 95%; CI 1,09–1,65) и 2,1 (доверительный интервал 95%; CI 1,5–2,9) соответственно [15].
В популяционном исследовании (n=1177) женщин c ожирением, молодого возраста (< 45 лет) было выявлено, что такие пациентки имеют более высокую вероятность возникновения опухолей молочной железы, подтвержденных гистологически и негативных по отношению к рецепторам эстрогена [16]. Существует мнение, что сахарный диабет является фактором риска возникновения эстроген-отрицательного РМЖ [17]. Таким образом, рост заболеваемости метаболического синдрома, сахарного диабета, ожирения может стимулировать увеличение количества пациенток с РМЖ [17].
Цель исследования: демонстрация редкого клинического случая лечения трижды негативного рака молочный железы у пациентки с метаболическим синдромом.
Клинический случай
Пациентка П., 60 лет находилась на лечении в клинике АО «Медицина» по поводу РМЖ.
Из анамнеза: в феврале 2016 году при ультразвуковом исследовании в правой молочной железе, в нижнем-наружном квадранте было выявлено образование 25х19 мм, неоднородной структуры с неровными контурами. Также в правой подмышечной и правой подключичной областях визуализировались конгломераты лимфатических узлов диаметром от 16 до 29 мм.
В медицинском учреждении по месту жительства пациентке П. была выполнена биопсия опухоли молочной железы. При гистологическом анализе биоптатов был выявлен инвазивный неспецифический рак молочной железы 3 степени злокачественности. Иммунногистохимический анализ опухоли показал отсутствие экспрессии к рецепторам эстрогена и прогестерона, экспрессию эпидермального фактора роста – слабое мембранное окрашивание более 10% опухолевых клеток (1+), пролиферативная активность опухоли (Ki‑67) – 86%, цитокератин 5–40%, экспрессия к рецепторам андрогенов – 5 баллов, полиморфизма генов BRCA 1,2 не выявлено.
Anamnesis vitae был осложнен сопутствующей: стенозирующий атеросклероз сосудов головного мозга, хроническая церебро-васкулярная недостаточность 3 степени, остаточные явления перенесенного инсульта в правой гемисфере (2007 г.). Гипертоническая болезнь 3 степени, нормотензия. Сахарный диабет, инсулинозависимый (25 ЕД/сут).
Учитывая злокачественную природу опухоли молочной железы, пациентка П. нуждалась в специальном лечении. Однако, в диспансере по месту жительства из-за тяжелой сопутствующей патологии в проведении химиотерапии было в нем отказано в связи с высокими рисками развития осложнений.
Объективно: состояние пациентки средней тяжести. Кожные покровы бледные. ИМТ 29 кг/м2. Левосторонний гемипарез с преобладанием снижения чувствительности в нижней конечности, гемидистония слева. Дыхание свободное, тоны сердца приглушены, ритмичные, ЧСС 82 в минуту, АД 130/80 мм рт ст.. Живот мягкий, безболезненный во всех отделах.
Status localis. Правая молочная железа отечная. Кожные покровы гиперемированы. В правом нижнем-наружном квадранте пальпируется опухоль до 3,0 см в диаметре, плотной консистенции. В подмышечной области справа конгломерат л/узлов до 3,5 см в диаметре.
Пациентка дообследована в клинике АО «Медицина»: КТ грудной клетки, сцинтиграфия костей скелета, КТ брюшной полости (ПЭТ-КТ на этом этапе диагностики не выполнялось из-за высокого уровня глюкозы крови) – данных об отдаленных метастазах не получено.
На основании данных инструментального исследования пациентке П. был установлен клинический диагноз: трижды негативный рак правой молочной железы, отечно-инфильтративная форма, стадия IIIC cT4bN3M0.
Учитывая тяжелую сопутствующую патологию в клинике АО «Медицина» проведен консилиум в составе: онколог, эндокринолог, невролог, кардиолог. Было решено провести лечение в несколько этапов:
- системная химиотерапия;
- хирургическое лечение;
- адъювантная лучевая терапия по стандартной программе.
В системную химиотерапию (ХТ) было включено 4 курса химиопрепаратов (1 раз в 3 недели) по схеме АС (доксорубицин + циклофосфан). Далее – 12 еженедельных введений Паклитаксела 80 мг/м2+ Карбоплатин 2 AUC. Курсы химиотерапии у пациентки П. проводились на фоне Дексаметазона 20 мг.
После завершения курса ХТ, через 7 месяцев пациентке было выполнено хирургическое лечение в объеме радикальной мастэктомии справа. Гистологический диагноз: инвазивный рак неспецифического типа на границе нижне-медиального и нижне-латерального секторов молочной железы с лечебным патоморфозом 3‑ей степени ткани опухоли. Метастазы в 2 из 7 регионарных лимфатических узлах 1‑го и 2‑го уровня с инфильтрацией их капсулы и окружающей жировой клетчатки с лечебным патоморфозом 2‑й степени. В краях резекции опухолевого роста не выявлено. В остальных участках молочной железы – признаки пролиферативной мастопатии и фиброзного аденоза, липоматоз и синусного гистиоцитоза. Реактивная гиперплазия лимфоузлов. Заключение: pуT2N1аMx, стадия IIB (по Lakhani S. R., 2012). Результаты ИГХ представлены в таблице 1. Молекулярно-генетический тип рака молочной железы определить нельзя ввиду выраженного лечебного патоморфоза.
Таблица 1. Динамика показателей ИГХ у наблюдаемой пациентки
Table 1. Dynamics of IHC indicators in the observed patient

При выполнении ПЭТ-КТ очагов с высокой метаболической активностью в мягких тканях грудной клетки зарегистрировано не было (рис. 1).
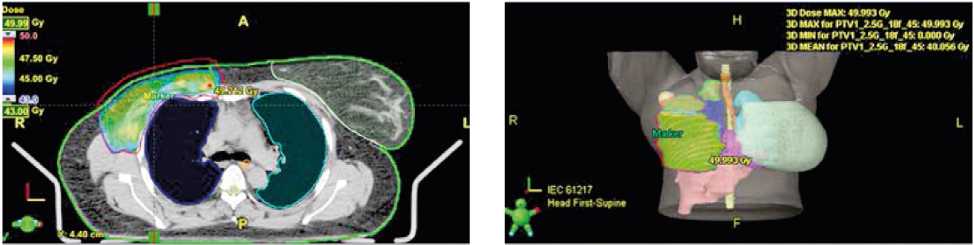
Рис. 1. ПЭТ-КТ с контрастированием 18F-фтордезоксиглюкозы после радикальной мастэктомии справа.
Fig. 1. PET-CT with contrast 18F-fluorodeoxyglucose after radical mastectomy on the right side.
После хирургического лечения РМЖ, как было и запланировано, пациентке П. была выполнена адъювантная лучевая терапия по стандартной программе. На фоне лучевой терапии у больной послеоперационная рана заживала вторичным натяжением.
Так как в лечении РМЖ наметилась положительная динамика, пациентка перенесла лечение хорошо, то с целью профилактики рецидива опухоли в феврале 2017 года было решено провести цитостатическую терапию капецитабином (6 курсов).
В настоящее время пациентка жива, компенсирована по сопутствующей патологии, по данным контрольного обследования – РМЖ без прогрессирования.
ОБСУЖДЕНИЕ
Женщины с диабетом, особенно в менопаузальный период, подвержены более высокому риску развития РМЖ [17][18]. Трижды негативный РМЖ представляет собой гетерогенную группу опухолей, для которых характерно агрессивное клиническое течение, более высокая частота рецидивов и низкая общая выживаемость в условиях метастазирования по сравнению с другими подтипами рака молочной железы [9]. Прогноз общей выживаемости у пациенток с трижды негативным РМЖ (отрицательный по экспрессии к рецепторам эстрогена, прогестерона и эпидермального фактора роста 2) на фоне метаболических нарушений и высокого ИМТ значительно ухудшается [19].
Как указывалось выше, метаболическое ожирение может быть самостоятельным фактором риска РМЖ [14][15]. Однако, сам инсулин индуцирует активность ароматазы жировой ткани и выработку эстрогена, а также непосредственно стимулирует рост и инвазию атипичных клеток молочной железы [20][21]. Нельзя забывать о воспалении жировой ткани, часто возникающем при ожирении и сахарном диабете 2 типа, при котором активизируются макрофаги и вырабатываются противовоспалительные цитокины и простагландин Е2 [3][20][22]. Эти процессы также индуцируют повышенную экспрессию ароматазы. Исследования на животных моделях показали, что противовоспалительные медиаторы и моноцитарный хемоаттрактантный протеин‑1 стимулируют пролиферацию и инвазию опухолевых клеток, и способствуют опухолевому ангиогенезу [21][22].
ЗАКЛЮЧЕНИЕ
Основное понимание патогенеза трижды негативного рака молочной железы в течение последних нескольких лет привело к значительному прогрессу в разработке стратегии полихимиотерапии и комбинированных методов лечения. Не смотря на тяжелую сопутствующую патологию у наблюдаемой нами пациентки, мы получили положительный результат многоступенчатой терапии, где цитотоксическая химиотерапия была базовым лечением для женщины с трижды негативным раком молочной железы.
Список литературы
1. Lebert JM, Lester R, Powell E, Seal M, McCarthy J. Advances in the systemic treatment of triple-negative breast cancer. Curr Oncol. 2018 Jun;25(Suppl 1):S142–S150. https://doi.org/10.3747/co.25.3954
2. Ройтберг Г.Е., Кондратова Н.В. Скрининг и профилактика рака молочной железы в работе врача первичного звена. Вестник Росздравнадзора. 2018;(1):57–61.
3. Асташов В.В., Волкова М.С., Казаков О.В., Иванова Е.Б., Ларионов П.М., Чепик В.И. и др. Регионарное лимфатическое русло при экспериментальной индукции опухоли молочной железы в условиях профилактической фитотерапии. Жизнь без опасностей. Здоровье. Профилактика. Долголетие. 2012;7(2):109–115.
4. Владимирова Л.Ю., Сторожакова А.Э., Снежко Т.А., Страхова Л.К., Абрамова Н.А., Кабанов С.Н. и др. Гормоноположительный HER2-негативный метастатический рак молочной железы: принятие решений в реальной клинической практике. Южно-российский онкологический журнал. 2020;1(2):46–51. https://doi.org/10.37748/2687-0533-2020-1-2-6
5. Jhan J-R, Andrechek ER. Triple-negative breast cancer and the potential for targeted therapy. Pharmacogenomics. 2017 Nov;18(17):1595–1609. https://doi.org/10.2217/pgs-2017-0117
6. Ходорович О.С., Снигирева Г.П., Чхиквадзе В.Д., Оксанчук Е.А., Меских Е.В., Новикова Е.И. BRCA- ассоциированный рак молочной железы. Случай из практики. Трудный пациент. 2016;14(10-11):46–49.
7. Siegel RL, Miller KD, Jemal A. Cancer Statistics, 2017. CA Cancer J Clin. 2017 Jan;67(1):7–30. https://doi.org/10.3322/caac.21387
8. Dent R, Trudeau M, Pritchard KI, Hanna WM, Kahn HK, Sawka CA, et al. Triple-negative breast cancer: clinical features and patterns of recurrence. Clin Cancer Res. 2007 Aug 1;13(15 Pt 1):4429–4434. https://doi.org/10.1158/1078-0432.CCR-06-3045
9. Abramson VG, Lehmann BD, Ballinger TJ, Pietenpol JA. Subtyping of triple-negative breast cancer: implications for therapy. Cancer. 2015 Jan 1;121(1):8–16. https://doi.org/10.1002/cncr.28914
10. Кит О.И., Попова Н.Н., Шихлярова А.И., Франциянц Е.М., Моисеенко Т.И., Меньшенина А.П. и др. Развитие посткастрационного синдрома и корригирующее действие ксенона в экспоненциальном дозовом режиме у пациенток молодого возраста с онкопатологией репродуктивных органов. Южно-российский онкологический журнал. 2020;1(3):6–17. https://doi.org/10.37748/2687-0533-2020-1-3-1
11. Savci-Heijink CD, Halfwerk H, Hooijer GKJ, Horlings HM, Wesseling J, van de Vijver MJ. Retrospective analysis of metastatic behaviour of breast cancer subtypes. Breast Cancer Res Treat. 2015 Apr;150(3):547–557. https://doi.org/10.1007/s10549-015-3352-0
12. Секундова М.А., Сдвижков А.М., Яковенко И.Ю. Трижды негативный рак молочной железы – особенности лечения. Паллиативная медицина и реабилитация. 2017;(4):13–18.
13. Foulkes WD, Smith IE, Reis-Filho JS. Triple-negative breast cancer. N Engl J Med. 2010 Nov 11;363(20):1938–1948. https://doi.org/10.1056/NEJMra1001389
14. Friedenreich CM. Physical activity and breast cancer: review of the epidemiologic evidence and biologic mechanisms. Recent Results Cancer Res. 2011;188:125–139. https://doi.org/10.1007/978-3-642-10858-7_11
15. Whiteman MK, Hillis SD, Curtis KM, McDonald JA, Wingo PA, Marchbanks PA. Body mass and mortality after breast cancer diagnosis. Cancer Epidemiol Biomarkers Prev. 2005 Aug;14(8):2009–2014. https://doi.org/10.1158/1055-9965.EPI-05-0106
16. Daling JR, Malone KE, Doody DR, Johnson LG, Gralow JR, Porter PL. Relation of body mass index to tumor markers and survival among young women with invasive ductal breast carcinoma. Cancer. 2001 Aug 15;92(4):720–729. https://doi.org/10.1002/1097-0142(20010815)92:4<720::aid-cncr1375>3.0.co;2-t
17. Wolf I, Sadetzki S, Gluck I, Oberman B, Ben-David M, Papa MZ, et al. Association between diabetes mellitus and adverse characteristics of breast cancer at presentation. Eur J Cancer. 2006 May;42(8):1077–1082. https://doi.org/10.1016/j.ejca.2006.01.027
18. Ройтберг Г.Е., Ушакова Т.И., Шархун О.О., Дорош Ж.В. Интегральный подход к диагностике метаболического синдрома в клинической практике. Кардиология. 2012;52(10):45–50.
19. Phipps AI, Malone KE, Porter PL, Daling JR, Li CI. Body size and risk of luminal, HER2-overexpressing, and triple-negative breast cancer in postmenopausal women. Cancer Epidemiol Biomarkers Prev. 2008 Aug;17(8):2078–2086. https://doi.org/10.1158/1055-9965.EPI-08-0206
20. Титов К.С., Казаков А.М., Барышникова М.А., Рябчиков Д.А., Чулкова С.В., Зарьянов Д.А. Некоторые молекулярные и иммунологические факторы прогноза трижды негативного рака молочной железы. Онкогинекология. 2019;4(32):26–34.
21. Rose DP, Gracheck PJ, Vona-Davis L. The Interactions of Obesity, Inflammation and Insulin Resistance in Breast Cancer. Cancers (Basel). 2015 Oct 26;7(4):2147–2168. https://doi.org/10.3390/cancers7040883
22. Barbarroja N, Lopez-Pedrera C, Garrido-Sanchez L, Mayas MD, Oliva-Olivera W, Bernal-Lopez MR, et al. Progression from high insulin resistance to type 2 diabetes does not entail additional visceral adipose tissue inflammation. PLoS One. 2012;7(10):e48155. https://doi.org/10.1371/journal.pone.0048155
Об авторах
Г. Е. РойтбергРоссия
Ройтберг Григорий Ефимович – академик РАН, д.м.н., профессор, заведующий кафедрой терапии, общей врачебной практики и ядерной медицины; президент клиники
SPIN: 1032-9122, AuthorID: 218525
117997, г. Москва, ул. Островитянова, д. 1
125047, г. Москва, 2-й Тверской-Ямской пер., д. 10
Ж. В. Дорош
Россия
Дорош Жанна Вадентиновна – к.м.н., доцент кафедры терапии, общей врачебной практики и ядерной медицины
SPIN: 3592-4274, AuthorID: 663889
117997, г. Москва, ул. Островитянова, д. 1
О. Ю. Аникеева
Россия
Аникеева Ольга Юрьевна – д.м.н., главный врач онкоцентра клиники
SPIN: 7581-8769, AuthorID: 696308
125047, г. Москва, 2-й Тверской-Ямской пер., д. 10
Рецензия
Для цитирования:
Ройтберг Г.Е., Дорош Ж.В., Аникеева О.Ю. Лечение трижды негативного рака молочный железы у пациентки с метаболическим синдромом. Research'n Practical Medicine Journal. 2021;8(1):62-68. https://doi.org/10.17709/2409-2231-2021-8-1-6
For citation:
Roitberg G.E., Dorosh J.V., Anikeeva O.Yu. Treatment of thrice-negative breast cancer in a patient with metabolic syndrome. Research and Practical Medicine Journal. 2021;8(1):62-68. (In Russ.) https://doi.org/10.17709/2409-2231-2021-8-1-6


























